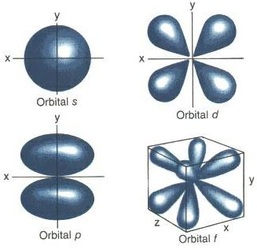
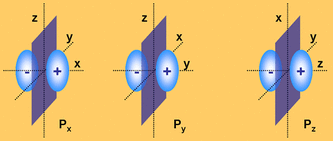
Función de Onda en un átomo polielectrónico
Un átomo polielectrónico es aquél que tiene más de un electrón.
En un átomo con un sólo electrón, en el que se considera al núcleo fijo en el origen de coordenadas, la ecuación de Schrödinger depende de las tres coordenadas, cartesianas o esféricas, del electrón. En un átomo polielectrónico de N electrones, la correspondiente ecuación de Schrödinger contiene 3N coordenadas, tres por cada uno de los electrones presentes en el átomo.
La ecuación de Schrödinger de un átomo polielectrónico debe tener en cuenta la atracción coulombiana del núcleo hacia todos y cada uno de los electrones, así como las repulsiones de cada uno de los electrones hacia todos los restantes.
La complejidad de un sistema de esta naturaleza hace inviable la solución analítica de las ecuaciones de Schrödinger correspondientes a estos átomos. No puede resolverse analíticamente la ecuación de Schrödinger ni siquiera para el átomo de helio.
El modelo aproximado que se utiliza para describir las propiedades de los electrones en los átomos se denomina aproximación orbital o método del orbital.
En este modelo se supone que las funciones de onda de un átomo polielectrónico pueden escribirse como el producto de N funciones de onda, una por cada uno de los electrones presentes en el átomo.
Ψ= ψ(1) + ψ(2) + ψ(3)……+ψ(N)
Esta aproximación sería correcta si los electrones fueran independientes uno de otro; es decir, si no interaccionaran entre ellos.
En el modelo de la aproximación orbital, el problema de cuantificar las repulsiones interelectrónicas se simplifica de la siguiente manera:
- Se supone que un electrón particular se encuentra sometido a la atracción del núcleo de carga +Ze, y a la repulsión global de los Z - 1 electrones restantes.
- Por otra parte, se supone que la distribución espacial de estos Z - 1 electrones restantes es de simetría esférica, y por tanto, asimilable a una sola carga negativa formalmente localizada en el núcleo
Con estas hipótesis, un electrón particular (al igual que el electrón del átomo de hidrógeno, o de los átomos hidrogenoides) se encuentra sometido a la acción de un campo de fuerzas centrales generado por la carga positiva +Ze del núcleo, y a una carga negativa resultante del efecto de los Z - 1 electrones restantes. El problema radica en la evaluación cuantitativa de esta carga negativa.
• El problema de evaluar la carga negativa equivalente a los restantes electrones se complica debido a las complejas distribuciones espaciales que presentan las funciones de onda hidrogenoides. Si todos y cada uno de los electrones estuvieran distribuidos sobre superficies esféricas concéntricas sería fácil calcular la carga efectiva a la que se encuentra sometido un electrón particular. De esta manera, el electrón más externo de un átomo de N electrones (número atómico Z = N) estaría sometido a un campo de fuerzas centrales generado por Z - (Z - 1) cargas positivas.
Por definición, la carga nuclear efectiva, Zefectiva, que actúa sobre un electrón particular se escribe de la siguiente forma:
Zefectiva= Z σ
en donde Z es la carga nuclear real del átomo (número de protones), y σ es la llamada constante de apantallamiento que cuantifica el efecto del resto de electrones.
Para utilizar las funciones de onda hidrogenoides en los átomos polielectrónicos, y dentro de la aproximación orbital, sólo se debe reemplazar Z por Zefectiva. El número atómico Z sólo aparece en la parte radial de las funciones de onda hidrogenoides; en consecuencia, sólo éstas se modifican en la aproximación orbital. Las partes angulares no se modifican debido a la hipótesis de considerar las repulsiones interelectrónicas de simetría esférica.
En un átomo con un sólo electrón, en el que se considera al núcleo fijo en el origen de coordenadas, la ecuación de Schrödinger depende de las tres coordenadas, cartesianas o esféricas, del electrón. En un átomo polielectrónico de N electrones, la correspondiente ecuación de Schrödinger contiene 3N coordenadas, tres por cada uno de los electrones presentes en el átomo.
La ecuación de Schrödinger de un átomo polielectrónico debe tener en cuenta la atracción coulombiana del núcleo hacia todos y cada uno de los electrones, así como las repulsiones de cada uno de los electrones hacia todos los restantes.
La complejidad de un sistema de esta naturaleza hace inviable la solución analítica de las ecuaciones de Schrödinger correspondientes a estos átomos. No puede resolverse analíticamente la ecuación de Schrödinger ni siquiera para el átomo de helio.
El modelo aproximado que se utiliza para describir las propiedades de los electrones en los átomos se denomina aproximación orbital o método del orbital.
En este modelo se supone que las funciones de onda de un átomo polielectrónico pueden escribirse como el producto de N funciones de onda, una por cada uno de los electrones presentes en el átomo.
Ψ= ψ(1) + ψ(2) + ψ(3)……+ψ(N)
Esta aproximación sería correcta si los electrones fueran independientes uno de otro; es decir, si no interaccionaran entre ellos.
En el modelo de la aproximación orbital, el problema de cuantificar las repulsiones interelectrónicas se simplifica de la siguiente manera:
- Se supone que un electrón particular se encuentra sometido a la atracción del núcleo de carga +Ze, y a la repulsión global de los Z - 1 electrones restantes.
- Por otra parte, se supone que la distribución espacial de estos Z - 1 electrones restantes es de simetría esférica, y por tanto, asimilable a una sola carga negativa formalmente localizada en el núcleo
Con estas hipótesis, un electrón particular (al igual que el electrón del átomo de hidrógeno, o de los átomos hidrogenoides) se encuentra sometido a la acción de un campo de fuerzas centrales generado por la carga positiva +Ze del núcleo, y a una carga negativa resultante del efecto de los Z - 1 electrones restantes. El problema radica en la evaluación cuantitativa de esta carga negativa.
• El problema de evaluar la carga negativa equivalente a los restantes electrones se complica debido a las complejas distribuciones espaciales que presentan las funciones de onda hidrogenoides. Si todos y cada uno de los electrones estuvieran distribuidos sobre superficies esféricas concéntricas sería fácil calcular la carga efectiva a la que se encuentra sometido un electrón particular. De esta manera, el electrón más externo de un átomo de N electrones (número atómico Z = N) estaría sometido a un campo de fuerzas centrales generado por Z - (Z - 1) cargas positivas.
Por definición, la carga nuclear efectiva, Zefectiva, que actúa sobre un electrón particular se escribe de la siguiente forma:
Zefectiva= Z σ
en donde Z es la carga nuclear real del átomo (número de protones), y σ es la llamada constante de apantallamiento que cuantifica el efecto del resto de electrones.
Para utilizar las funciones de onda hidrogenoides en los átomos polielectrónicos, y dentro de la aproximación orbital, sólo se debe reemplazar Z por Zefectiva. El número atómico Z sólo aparece en la parte radial de las funciones de onda hidrogenoides; en consecuencia, sólo éstas se modifican en la aproximación orbital. Las partes angulares no se modifican debido a la hipótesis de considerar las repulsiones interelectrónicas de simetría esférica.